
Tabella dei contenuti
Sicurezza dei pazienti
Una terapia dovrebbe essere più efficace e sicura possibile. Tuttavia, nessun medicamento è completamente privo di rischi. Pertanto, vengono utilizzati solo i medicamenti i cui benefici superano i rischi. Per conoscere con precisione i possibili rischi di un medicamento e per ridurli il più possibile, sia il produttore che l'autorità competente fanno grandi sforzi. Per essere omologato, un medicamento viene prima sottoposto a numerosi test. Nel seguente articolo scoprite quali sono queste fasi e quale importante contributo potete dare come pazienti.
Il percorso per medicamenti sicuri
La sicurezza dei pazienti ha la massima priorità. Pertanto, i medicamenti vengono omologati per la vendita solo se sono efficaci e sicuri. La sicurezza dei medicamenti continua a essere monitorata anche dopo l’ingresso sul mercato.
Con tutti i medicamenti, oltre all’effetto terapeutico desiderato, possono verificarsi anche effetti indesiderati, i cosiddetti effetti collaterali, come mal di testa o nausea. Purtroppo, quindi, nessun medicamento è completamente privo di rischi. Tuttavia, è fondamentale che il beneficio di un medicamento sia significativamente superiore al suo rischio. Solo i medicamenti con un cosiddetto rapporto beneficio-rischio positivo sono omologati per l’uso nei pazienti. Inoltre, rimangono sul mercato solo finché questo è assicurato.
Per garantire che un medicamento offra ai pazienti la maggiore sicurezza possibile, viene testato e monitorato durante tutte le sue «fasi di vita».
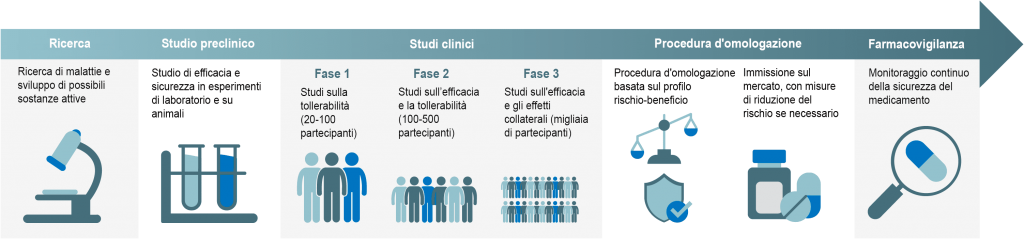
Prima dell'omologazione: analisi di laboratorio e studi
Un nuovo medicamento è il risultato di anni di ricerca e sviluppo. La sicurezza gioca un ruolo importante sin dall’inizio di questo processo. Molto prima di essere considerato per l’uso negli esseri umani, un principio attivo viene prima accuratamente testato in provetta, su colture cellulari e in esperimenti su animali. Tra le altre cose, gli sviluppatori verificano se il suo uso a breve o a lungo termine è tossico, quale dose è ottimale, come il principio attivo viene degradato nel corpo e se ha un effetto sulla fertilità o sullo sviluppo embrionale.
Molti potenziali principi attivi vengono scartati in questa prima fase di sviluppo perché i test mostrano che i principi attivi non sarebbero abbastanza sicuri. Solo le sostanze che si sono dimostrate valide possono essere testate sugli esseri umani. Questi cosiddetti studi clinici durano generalmente tanti anni. Si distinguono tre fasi, con il numero di soggetti di test che aumenta di fase in fase. Negli studi clinici finali di fase 3, di solito partecipano migliaia, a volte anche diverse decine di migliaia di pazienti. Oltre a provare l’efficacia, l’obiettivo è quello di conoscere meglio il profilo di sicurezza del medicamento e di scoprire gli effetti collaterali.
Gli studi clinici rappresentano un grande ostacolo per i potenziali medicamenti. In questa fase molti principi attivi candidati vengono scartati. Ciò può accadere per molte ragioni. Spesso l’efficacia non è sufficiente. Oppure compaiono effetti indesiderati negli esseri umani che sono sproporzionati rispetto all’efficacia e non erano ancora evidenti negli esperimenti sugli animali. Solo i medicamenti che si sono dimostrati validi attraverso tutte le fasi degli studi clinici sono finalmente omologati dall’autorità competente per l’uso nella pratica.
Omologazione da parte dell'istituto per gli agenti terapeutici
L’istituto svizzero per gli agenti terapeutici Swissmedic valuta attentamente ogni domanda di omologazione di un medicamento. A tal fine, analizza tutti i dati di studio raccolti e decide se il medicamento è sicuro ed efficace. Swissmedic determina anche quali misure devono essere attuate per limitare al massimo i rischi identificati.
Le misure importanti per aumentare la sicurezza del paziente variano molto a seconda del medicamento. Di seguito sono riportati alcuni esempi.
- Alcuni medicamenti possono essere dispensati solo su prescrizione medica (obbligo di prescrizione).
- Gli operatori sanitari e i pazienti sono ben informati sui rischi (ad es. attraverso il foglietto illustrativo).
- I medici che usano il medicamento devono monitorare regolarmente i valori del sangue dei loro pazienti o fare altri esami.
- I pazienti ricevono materiali di formazione o un passaporto del paziente con informazioni importanti sul loro trattamento o istruzioni per l’uso.
Immaginate un medicamento X che potrebbe essere pericoloso per il nascituro se preso durante la gravidanza. Per minimizzare questo rischio, il foglietto illustrativo indicherebbe che durante il trattamento deve essere usato un metodo contraccettivo sicuro. Inoltre, il medicamento X richiederebbe una prescrizione, cioè sarebbe disponibile solo con la prescrizione di un medico.
Generalmente ci vuole più di un anno dalla presentazione della domanda di omologazione prima che Swissmedic decida. Tuttavia, questa verifica dettagliata secondo direttive rigorose è fondamentale. Essa garantisce che in Svizzera vengano commercializzati solo i medicamenti sufficientemente sicuri per gli utenti. Solo dopo che Swissmedic ha rilasciato una decisione di omologazione positiva, i medici possono prescrivere un medicamento per lo scopo terapeutico previsto.
I medicamenti vengono omologati solo quando la loro sicurezza è stata ampiamente testata e i loro benefici superano i potenziali rischi.
Tabella dei contenuti
Dopo l'omologazione: farmacovigilanza
Anche dopo l’omologazione e il lancio sul mercato, i produttori di medicamenti devono monitorare continuamente la sicurezza di ogni loro medicamento. Questo processo si chiama farmacovigilanza (dal latino «vigilantia» per «vigilanza») e si svolge in stretta collaborazione con Swissmedic, l’istituto svizzero per gli agenti terapeutici. La farmacovigilanza comprende tutte le misure volte a monitorare, valutare e comprendere gli effetti indesiderati dei medicamenti e, dunque, aiutare a prevenirli.
Queste misure includono, ad esempio, l’obbligo per medici e farmacisti di segnalare effetti collaterali ignoti o gravi. Queste cosiddette segnalazioni spontanee costituiscono una parte importante della farmacovigilanza. Possono essere fatte non solo dagli operatori sanitari, ma anche dai pazienti stessi. Inoltre, a volte sono condotti ulteriori studi e analisi mirati anche dopo che un medicamento è stato omologato per saperne di più sulla sua sicurezza nell’uso quotidiano.
Perché la sicurezza di un medicamento viene ulteriormente esaminata dopo l'entrata sul mercato, se vengono omologati solo i medicamenti testati?
Forse anche voi vi state ponendo questa legittima domanda. La ragione del monitoraggio continuo della sicurezza è questa: anche gli studi di omologazione su larga scala non possono escludere la possibilità che un effetto collaterale possa passare inosservato. Sebbene la maggior parte degli effetti collaterali vengano identificati negli studi clinici, gli effetti collaterali estremamente rari a volte sfuggono. Infine, il gruppo di partecipanti allo studio, non importa quanto grande, rappresenta sempre un campione. L’effetto dei medicamenti può variare invece da persona a persona. Inoltre, gli effetti collaterali che si verificano solo quando un medicamento viene assunto per un periodo di tempo molto lungo sono difficili da riconoscere negli studi clinici perché gli studi hanno una durata limitata. Per questi e altri motivi è così importante continuare a monitorare i medicamenti anche dopo l’omologazione.
Le misure per garantire la sicurezza di un medicamento non sono sempre state così ampie come lo sono oggi. Per questo ci sono stati tragici incidenti in passato, che dimostrano quanto siano importanti la farmacovigilanza e una regolamentazione rigorosa per l’omologazione dei medicamenti.
Uno di questi esempi è un sonnifero che era disponibile sul mercato senza prescrizione negli anni ’50. Quando è stato introdotto sul mercato era considerato a basso rischio e veniva dato anche alle donne in gravidanza. Poiché all’epoca c’erano poche direttive per esaminare e monitorare la sicurezza dei medicamenti, non era una pratica comune verificare se un principio attivo potesse influire sulla vita del nascituro. Mancava inoltre la farmacovigilanza legalmente richiesta per il monitoraggio dopo l’approvazione alla commercializzazione.
Per questo motivo, solo anni dopo che il sonnifero era stato immesso sul mercato, è stato riconosciuto che potevano verificarsi malformazioni nel bambino se la madre assumeva il medicamento durante determinate settimane della gravidanza. Quando questa correlazione fu scoperta, il sonnifero fu immediatamente ritirato dal mercato nel 1961. In seguito, le direttive per lo sviluppo e l’omologazione dei medicamenti sono diventate molto più stringenti. Da allora in poi, è necessario dimostrare la sicurezza di un nuovo medicamento in modo rigoroso.
Ma questi requisiti sarebbero stati sufficienti per evitare la tragedia descritta sopra? Per rispondere a questa domanda, il principio attivo del sonnifero è passato attraverso gli esami di sicurezza che facevano parte del programma obbligatorio alla fine degli anni ’60. Si è scoperto che i test avrebbero indicato in modo affidabile il pericolo della sostanza per lo sviluppo dell’embrione. Quindi, se il principio attivo fosse stato scoperto solo dopo, l’omologazione come sonnifero non sarebbe stata certamente concessa. Un medicamento con un tale profilo di rischio può essere considerato solo per il trattamento di una malattia grave e altrimenti non trattabile e solo in combinazione con una rigorosa contraccezione e prescrizione.
L’incidente descritto ha portato all’introduzione di sistemi di farmacovigilanza in tutto il mondo. Questa è stata, per così dire, la «nascita» della farmacovigilanza, che permette oggi di individuare i nuovi effetti indesiderati di un medicamento in una fase precoce e di prendere rapidamente delle misure adeguate.
Per garantire la sicurezza dei pazienti, la tollerabilità dei medicamenti è continuamente monitorata anche dopo l’omologazione. I pazienti possono contribuire alla sicurezza dei medicamenti segnalando eventuali effetti collaterali.
Tabella dei contenuti
Cosa succede con le segnalazioni degli effetti collaterali
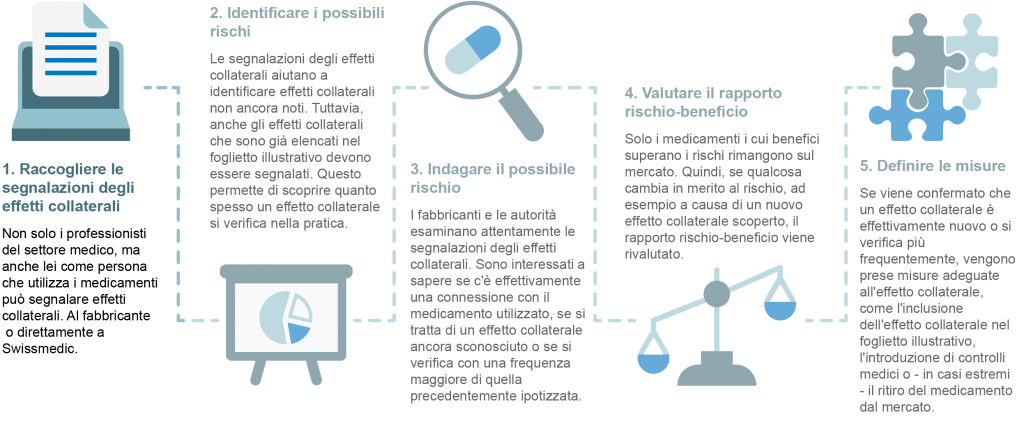
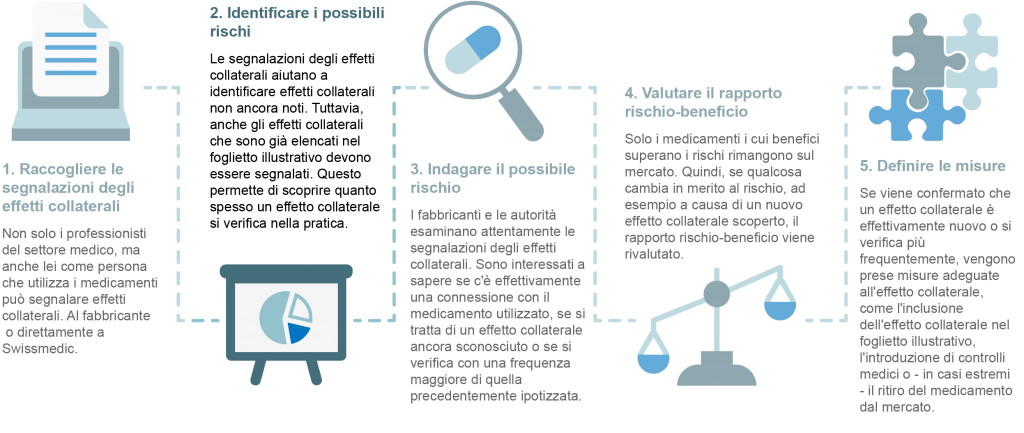
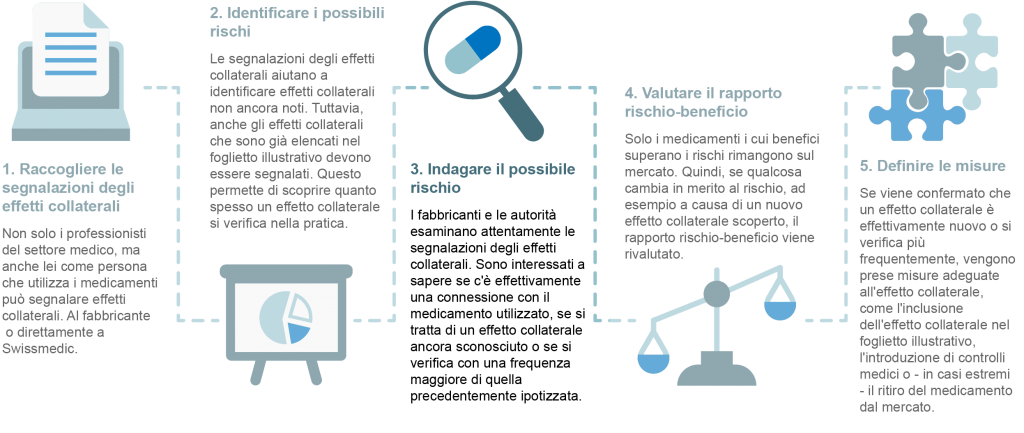
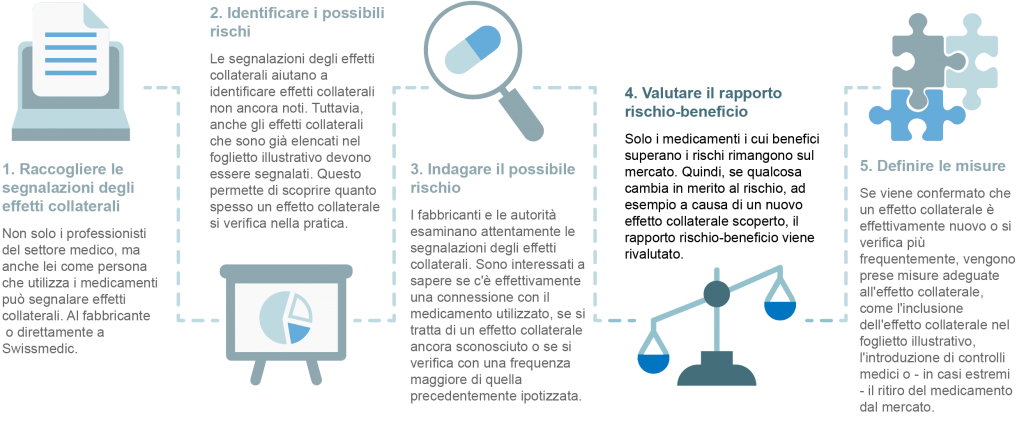
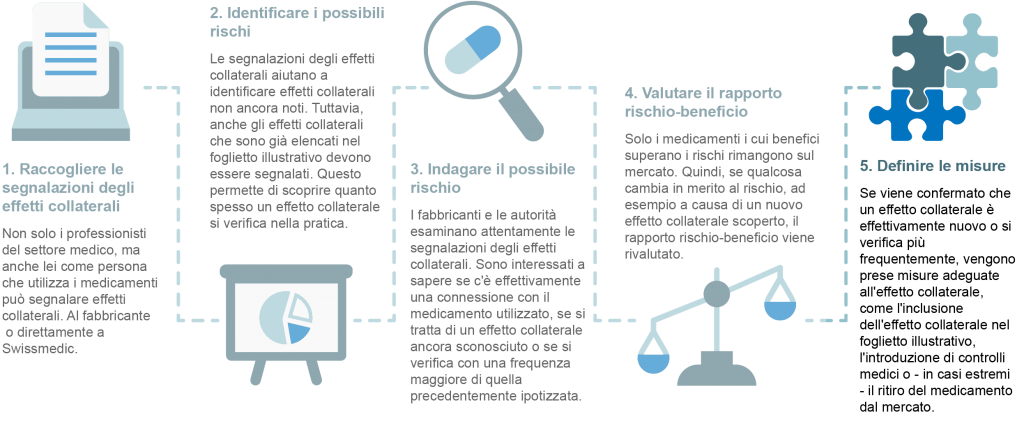
Per il monitoraggio continuo della sicurezza dei medicamenti, i produttori si basano sulla segnalazione degli effetti collaterali da parte degli operatori sanitari, ma anche dei pazienti. Tutte le segnalazioni di effetti collaterali vengono anonimizzate e analizzate dall’azienda produttrice e dall’istituto per gli agenti terapeutici per identificare potenziali nuovi rischi. Poiché i medicamenti sono usati in tutto il mondo, la loro sicurezza è una questione internazionale. Pertanto, tutti i casi sospetti segnalabili sono anche inseriti nel database dell’Organizzazione Mondiale della Sanità (OMS).
La sicurezza di un medicamento è quindi continuamente valutata da varie autorità. Se questa valutazione indica un cambiamento nel rapporto rischio-beneficio, le autorità responsabili e i produttori sono informati immediatamente in modo che possano essere prese le misure necessarie. Di seguito sono riportate alcune possibili misure.
- Un nuovo effetto collaterale o una nuova avvertenza sono inclusi nell’informazione professionale (per i medici) e nel foglietto illustrativo (per i pazienti).
- Vengono prodotti materiali di formazione per medici e/o pazienti.
- Vengono introdotti controlli medici supplementari.
- L’uso del medicamento viene limitato per alcuni gruppi di persone (ad es. le donne in gravidanza) o in caso di trattamento simultaneo con altri medicamenti.
- Nel peggiore dei casi, un medicamento viene ritirato dal mercato a causa della scoperta di nuovi rischi. Fortunatamente, questa azione drastica viene presa molto raramente nella pratica. Generalmente, infatti, i rischi dei medicamenti che vengono scoperti solo dopo l’approvazione alla commercializzazione possono essere contrastati da misure come quelle descritte sopra.
Affrontare correttamente gli effetti collaterali
Quando si usa un medicinale, è importante sapere come affrontare correttamente gli eventuali effetti collaterali. A tal fine, bisogna comprendere cosa sono esattamente gli effetti collaterali.
Generalmente i medicamenti agiscono su diverse parti dell’organismo umano e possono quindi causare diversi effetti. Oltre agli effetti desiderati, ci sono purtroppo a volte anche effetti indesiderati. Questi effetti indesiderati del medicamento sono chiamati effetti collaterali.
Alcuni effetti collaterali sono fisici, come eruzioni cutanee o tachicardia. Altri, invece, possono anche riguardare la psiche e manifestarsi, ad esempio, sotto forma di incubi. Finché gli effetti collaterali sono lievi, spesso il paziente non li nota. Possono però anche causare gravi disturbi e, a volte, diventare addirittura pericolosi per la persona colpita.
Tuttavia, non tutti i disturbi che si verificano durante la terapia sono necessariamente dovuti ai medicamenti assunti. Possono anche essere sintomi della malattia stessa o avere un’altra ragione. Pertanto, è importante consultare il medico in caso di disturbi nuovi o insoliti.
Discutete sempre gli effetti collaterali sospetti con un operatore sanitario.
Tabella dei contenuti
Frequenza degli effetti collaterali
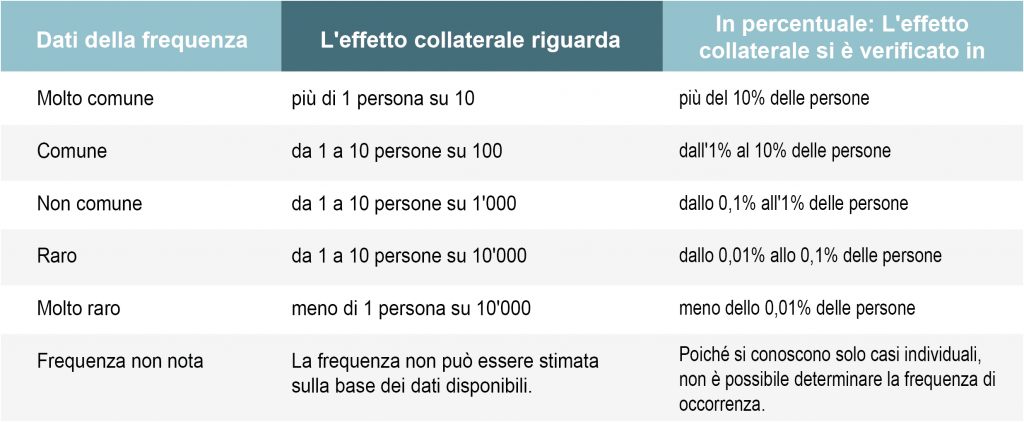
Gli effetti collaterali riscontrati con un particolare medicamento sono elencati nel foglietto illustrativo (se disponibile con il prodotto). È importante sapere che non per forza tutti gli effetti collaterali si verificano in tutte le persone trattate. Al contrario. La maggior parte degli effetti collaterali si nota solo in una piccola minoranza di persone che usano il medicamento. Di solito, se si manifestano, si hanno solo singoli effetti collaterali e non tutti quelli elencati. Le informazioni relative alla frequenza riportate nel foglietto illustrativo per ogni effetto collaterale elencato indicano quanti pazienti sono affetti mediamente dall’effetto collaterale e si basano sulla seguente scala:
Cosa fare in caso di effetti collaterali
Fate attenzione agli effetti collaterali e discutetene con il vostro medico.
Gli effetti collaterali sono una ragione frequente per cui i pazienti non seguono più le istruzioni del loro medico e interrompono il trattamento da soli. Tuttavia, interrompere una terapia in corso senza consultare lo specialista responsabile può rappresentare un serio rischio per la persona interessata. Inoltre, gli effetti collaterali possono spesso essere trattati in modo specifico e i sintomi possono essere alleviati. Pertanto, è importante prestare attenzione agli effetti collaterali e segnalarli allo specialista responsabile. Prendete nota di tutti gli effetti collaterali che avvertite e discutetene con il vostro medico durante la visita successiva. Insieme potete trattare i disturbi o cambiare la terapia. Se soffrite di gravi effetti collaterali, segnalateli immediatamente al vostro medico.
Segnalate gli effetti collaterali.
Segnalando gli effetti collaterali, potete contribuire a garantire che gli effetti collaterali ignoti o non adeguatamente descritti siano identificati ed esaminati.
Come segnalare gli effetti collaterali
Anche i pazienti possono segnalare gli effetti collaterali e contribuire a migliorare ulteriormente la qualità e la sicurezza dei medicamenti.
Segnalazione degli effetti collaterali
Gli effetti collaterali di tutti i medicamenti possono essere segnalati a Swissmedic tramite questo modulo. In alternativa, potete usare questo modulo Roche per segnalare gli effetti collaterali dei prodotti Roche.
Importante: discutete sempre eventuali effetti collaterali con il vostro medico per trattare i vostri disturbi o cambiare terapia.
Per segnalare gli effetti collaterali sono necessarie le seguenti informazioni.
- Informazioni sulla persona che segnala e sulla persona colpita (qualora non si tratti della stessa persona)
- Nome del medicamento
- Tipo di effetto collaterale o disturbo
- Più informazioni (ad es. i medicamenti concomitanti, la dose o il numero di lotto del medicamento) fornite sull’effetto collaterale, meglio potrà essere valutata la vostra segnalazione.
È possibile che la persona che gestisce la vostra segnalazione vi contatti per chiarire delle questioni e per valutare meglio la vostra segnalazione.
Come potete rendere il trattamento più sicuro
Anche come pazienti potete contribuire a garantire che il vostro trattamento sia il più sicuro e tollerabile possibile. La cosa più importante è che partecipiate attivamente e pensiate al vostro trattamento. Questo può avere un effetto molto positivo sul successo del vostro trattamento. Orientatevi ai seguenti principi.
- Fate domande se non capite qualcosa o se qualcosa vi preoccupa.
- Tenete aggiornati i vostri documenti, soprattutto un elenco di tutti i medicamenti che prendete attualmente, e portatelo con voi all’appuntamento.
- Coinvolgete attivamente i membri della famiglia o le persone che vi accompagnano. Queste persone possono sostenervi emotivamente e aiutarvi anche ascoltandovi e riflettendo con voi.
Pensando attivamente e chiarendo tutte le vostre domande, potete contribuire molto alla sicurezza del vostro trattamento.
Tabella dei contenuti
Di seguito trovate dei consigli su come potete contribuire al successo e alla sicurezza del vostro trattamento. Potete anche scaricare questi consigli in formato PDF e usarli come checklist durante il vostro trattamento.
Per ulteriori informazioni sul tema «Gestione sicura dei medicamenti», potete trovare → qui un opuscolo informativo della fondazione Sicurezza dei pazienti Svizzera, ordinabile anche come stampa tramite il loro → sito web.
Checklist: consigli per un trattamento più sicuro
Prima dell'appuntamento dal medico
- Prima di andare dal medico scrivete tutte le vostre domande e portatele con voi all’appuntamento.
- Portate con voi tutti i documenti necessari al vostro appuntamento.
- Un → piano di medicazione attuale che include tutti i medicamenti, anche i medicamenti e gli integratori acquistati autonomamente e a base di erbe.
- I vostri passaporti sanitari (passaporto del paziente, passaporto dei medicamenti, libretto delle vaccinazioni, ecc.)
- Referti di esami importanti di altri medici
- È meglio che qualcuno vicino a voi vi accompagni all’appuntamento con il medico per un sostegno (particolarmente importante in caso di barriere linguistiche).
Durante l'appuntamento dal medico
- Di seguito sono elencati gli argomenti importanti di cui parlare con il medico durante l’appuntamento.
- Se è incinta, sta pianificando una gravidanza a breve o sta allattando.
- Le sue patologie (comprese quelle per cui è in cura presso un altro medico).
- Informate il vostro medico sulle altre medicine che state assumendo (sulla base del vostro piano di medicazione) e fate controllare se tutti i medicamenti sono ancora utili.
- Allergie (in particolare a certi principi attivi farmaceutici) e intolleranze note.
- Effetti collaterali sperimentati durante il trattamento.
- Ponete tutte le vostre domande durante l’appuntamento con il vostro medico.
- Se non capite qualcosa, chiedete. Non vergognatevi di chiedere più di una volta se necessario.
- Può essere utile ripetere con parole vostre ciò che avete capito per verificare di aver capito tutto correttamente.
- Fatevi spiegare a cosa servono i medicamenti che ricevete. Informatevi sui rischi e sugli effetti collaterali del trattamento e se i medicamenti che state prendendo sono compatibili tra loro.
- Chiedete al medico di spiegarvi i risultati degli esami e le proposte di trattamento.
- Fatevi spiegare dal medico a cosa prestare attenzione e cosa potete fare voi stessi per supportare il trattamento.
- Prendete appunti durante l’appuntamento dal medico.
- Assicuratevi di capire esattamente come vanno usati i medicamenti.
- Se sospettate che qualcosa sia stato confuso durante il trattamento, parlatene con il personale sanitario.
- Fatevi dare un piano di medicazione con informazioni esatte sull’assunzione.
Dopo l'appuntamento dal medico
- Assicuratevi che in farmacia riceviate i medicamenti giusti.
- Osservate e annotate gli effetti collaterali sospetti e parlatene con il vostro medico. Se temete di soffrire di un grave effetto collaterale, segnalatelo immediatamente al vostro medico.
- Leggete attentamente i documenti che avete ricevuto dal vostro medico.
- Seguite attentamente le istruzioni per l’assunzione dei medicamenti.
- Chiedete ancora una volta se state ancora aspettando i risultati degli esami.
- Rispettate tutti gli appuntamenti per i trattamenti e gli esami.
- In caso di decisioni e interventi importanti, confrontatevi con i vostri parenti.
→ Scarica la checklist
I medicamenti vengono testati e monitorati rigorosamente durante tutte le loro «fasi di vita» per garantire che offrano la maggiore sicurezza possibile.